(1)电位法测定pH值的理论 把一只对氢离子H+可逆的电极和一只参比电极放人到溶液中,就组成了一个原电池。
因为原电池中参比电极的电位在必定条件下是不变的,那么原电池的电动势就会跟着被测溶液中氢离子的活度而改变。因而,能够经过丈量原电池的电动势,从而计算出溶液的pH值。因氢离子挑选电极契合能斯特方程,则电极电位为
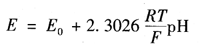
式中 Eo——氢电极的规范电位,规则该值等于0;
R——气体常数;
T——热力学温度;
F——法拉第常数。
式中,2.302,6RT/F被称为对氢离子可逆的电极理论电化转化系数。当被测溶液pH值改变1个单位时,因为R和F都是常数,因而电极电位便是温度的函数。
(2)电位法测定 pH值的有用界说 在丈量溶液pH值的原电池中,因为参比电极的电位随温度改变而改变,使得无液界电位的原电池设备结构杂乱,操作较困难。因而,pH值的丈量实际上选用的是有液界的原电池,也便是说,用已知规范pHs值溶液测定不知道pHx值的溶液。
当被测溶液为已知pH.规范溶液时,原电池电动势为
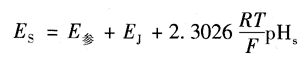
当被测溶液为不知道的pH,时,原电池电动势为
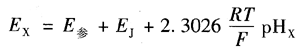
其间,E参是参比电极电位;Ej是指示电极电位。
若两次测定中E参和E,均坚持不变(测定中,必定条件下E参是不变的,E参的改变很小),则有:
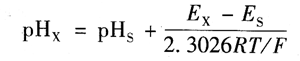
上式称为pH的有用界说,由此能够看出,pHs规范溶液是丈量的基准。